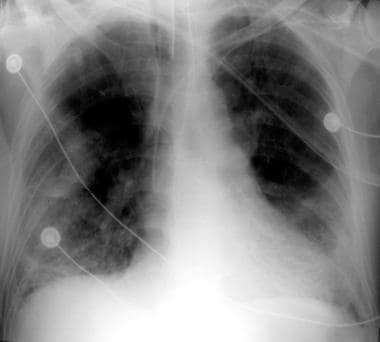
Los objetivos de la ventilación mecánica en el SDRA son mantener la oxigenación y evitar la toxicidad del oxígeno y las complicaciones de la ventilación mecánica. En general, esto implica mantener la saturación de oxígeno en el rango del 85-90%, con el objetivo de reducir la fracción inspirada de oxígeno (FiO 2 ) a menos del 65% dentro de las primeras 24-48 horas. Lograr este objetivo casi siempre requiere el uso de niveles moderados a altos de presión positiva al final de la espiración (PEEP).
Los estudios experimentales han demostrado que la ventilación mecánica puede promover un tipo de lesión pulmonar aguda denominada lesión pulmonar asociada a la ventilación mecánica. Una estrategia de ventilación protectora que utilice volúmenes corrientes bajos y presiones meseta limitadas mejora la supervivencia en comparación con los volúmenes corrientes y presiones convencionales.
En un estudio de ARDS Network, los pacientes con ALI y ARDS fueron asignados aleatoriamente a ventilación mecánica con un volumen corriente de 12 ml/kg de peso corporal previsto y una presión inspiratoria de 50 cm de agua o menos o con un volumen corriente de 6 ml/kg y una presión inspiratoria de 30 cm de agua o menos; el estudio se detuvo antes de tiempo después de que un análisis provisional de 861 pacientes demostrara que los sujetos del grupo de bajo volumen corriente tenían una tasa de mortalidad significativamente menor (31 % frente a 39,8 %). [ 46 ]
Mientras que estudios anteriores que emplearon volúmenes corrientes bajos permitieron que los pacientes estuvieran hipercápnicos (hipercapnia permisiva) y acidóticos para lograr los objetivos de ventilación protectora de volumen corriente bajo y presión inspiratoria baja en las vías respiratorias, el estudio ARDS Network permitió aumentos en la frecuencia respiratoria y la administración de bicarbonato para corregir la acidosis. Esto puede explicar el resultado positivo en este estudio en comparación con estudios anteriores que no habían logrado demostrar un beneficio.
Por lo tanto, se recomienda la ventilación mecánica con un volumen corriente de 6 ml/kg de peso corporal previsto, con ajuste del volumen corriente hasta 4 ml/kg si es necesario para limitar la presión de meseta inspiratoria a 30 cm de agua o menos. Aumente la frecuencia respiratoria y administre bicarbonato según sea necesario para mantener el pH en un nivel cercano a lo normal (7.3).
En el estudio ARDS Network, los pacientes ventilados con volúmenes corrientes más bajos necesitaron niveles más altos de PEEP (9,4 frente a 8,6 cm de agua) para mantener la saturación de oxígeno en un 85 % o más. Algunos autores han especulado que los niveles más altos de PEEP también pueden haber contribuido a las mejores tasas de supervivencia. Sin embargo, un ensayo posterior de ARDS Network de niveles más altos frente a niveles más bajos de PEEP en pacientes con SDRA no mostró ningún beneficio de los niveles más altos de PEEP en términos de supervivencia o duración de la ventilación mecánica. [ 47 ]
La falta de eficacia de niveles más altos de PEEP puede estar relacionada con el hecho de que los niveles recomendados de PEEP en el estudio ARDS Network se basaron en la oxigenación y no fueron individualizados en función de la mecánica pulmonar. El ARDS es un proceso no homogéneo y los pacientes pueden tener diferentes patrones de lesión pulmonar y diferente mecánica de la pared torácica. La medición de las presiones esofágicas con un catéter con balón esofágico permite estimar la presión transpulmonar. Basar la estrategia del respirador en estas presiones a medida que se titula la PEEP podría permitir la determinación de los “mejores niveles de PEEP” para mejorar la oxigenación y minimizar el volutrauma y la atelectasia. [ 48 ]
El uso de la estrategia de ventilación protectora de volúmenes corrientes más bajos, presión meseta limitada y PEEP más alta mejora la supervivencia en el SDRA. Amato et al, [ 49 ] a través de una revisión retrospectiva de más de 3500 pacientes con SDRA reportados en nueve estudios previos, encontraron que la variable de ventilación más importante para determinar la supervivencia es delta P (presión meseta menos PEEP). Delta P es un reflejo de la distensibilidad pulmonar y es confiable para predecir la supervivencia en pacientes con SDRA que no respiran espontáneamente. En estos pacientes, niveles más bajos de delta P mejoraron la supervivencia. Niveles más altos de PEEP y volúmenes corrientes más bajos no mejoraron la supervivencia, a menos que estuvieran asociados con niveles más bajos de delta P.
El uso de paralizantes sigue siendo controvertido. Los pacientes con SDRA grave también pueden beneficiarse del uso temprano de agentes bloqueadores neuromusculares. En un grupo de pacientes con SDRA grave (PaO2 / FiO2 < 120) diagnosticado dentro de las 48 horas, se demostró que la parálisis con cisatracurio durante las siguientes 48 horas mejoraba la mortalidad a 90 días, en comparación con placebo (31,6% para cisatracurio frente a 40,7% para placebo); aumentaba los días sin respirador y reducía el barotrauma. No hubo un aumento en la incidencia de debilidad muscular prolongada en el grupo que estuvo paralizado. [ 50 ] Sin embargo, un estudio más reciente en 2019 de pacientes con una relación PaO2 / FiO2 de menos de 150 mmHg durante menos de 48 horas no demostró ninguna mejora en la mortalidad, los días sin respirador o las tasas de barotrauma. [ 51 ] Los agentes bloqueadores neuromusculares deben usarse de forma selectiva. Estos agentes pueden ser beneficiosos en pacientes con SDRA muy grave, aquellos que tienen problemas para sincronizar la respiración con el ventilador y pacientes con poca distensibilidad pulmonar.
Los médicos no deben utilizar paralizantes en todos los casos, sino que deben utilizarlos sólo en aquellos en los que se espera que la duración de la ventilación supere unas pocas horas. Los pacientes no deben permanecer ventilados durante más tiempo del que tardan los paralizantes en hacer efecto. La duración de la parálisis dependerá de la afección. [ 50 ]
Un estudio de Jaber et al. examinó la debilidad diafragmática durante la ventilación mecánica junto con la relación entre la duración de la ventilación mecánica y la lesión o atrofia diafragmática. [ 52 ] El estudio determinó que los períodos más prolongados de ventilación mecánica se asociaron con una lesión significativamente mayor de las fibras ultraestructurales, un aumento de las proteínas ubiquitinadas, una mayor expresión del factor nuclear p65-kB, mayores niveles de proteasas activadas por calcio y una disminución del área transversal de las fibras musculares en el diafragma. La conclusión fue que la debilidad, la lesión y la atrofia pueden ocurrir rápidamente en los diafragmas de los pacientes con ventilación mecánica y están significativamente correlacionadas con la duración del soporte ventilatorio.
Vaya a Barotrauma y ventilación mecánica para obtener información completa sobre este tema.
Presión positiva al final de la espiración y presión positiva continua en las vías respiratorias
El síndrome de dificultad respiratoria aguda (SDRA) se caracteriza por una hipoxemia grave. Cuando no se puede mantener la oxigenación a pesar de las altas concentraciones de oxígeno inspirado, el uso de CPAP o PEEP suele favorecer una mejor oxigenación, lo que permite reducir gradualmente la FiO2 .
Con la PEEP, se mantiene una presión positiva durante toda la espiración, pero cuando el paciente inhala espontáneamente, la presión de las vías respiratorias disminuye por debajo de cero para activar el flujo de aire. Con la CPAP, se utiliza una válvula de demanda de baja resistencia para permitir que se mantenga una presión positiva de forma continua. La ventilación con presión positiva aumenta la presión intratorácica y, por lo tanto, puede reducir el gasto cardíaco y la presión arterial. Debido a que la presión media de las vías respiratorias es mayor con la CPAP que con la PEEP, la CPAP puede tener un efecto más profundo sobre la presión arterial.
En general, los pacientes toleran bien la CPAP, y se suele utilizar en lugar de la PEEP. Se cree que el uso de niveles adecuados de CPAP mejora los resultados en el síndrome de dificultad respiratoria aguda. Al mantener los alvéolos en un estado expandido durante todo el ciclo respiratorio, la CPAP puede reducir las fuerzas de cizallamiento que promueven la lesión pulmonar asociada al respirador.
El mejor método para determinar el nivel óptimo de CPAP en pacientes con SDRA es controvertido. Algunos están a favor del uso de CPAP suficiente para permitir la reducción de la FiO2 por debajo del 65%.
Otro enfoque, favorecido por Amato et al, es el llamado enfoque de pulmón abierto, en el que el nivel apropiado se determina mediante la construcción de una curva de volumen de presión estática. [ 53 ] Esta es una curva en forma de S, y el nivel óptimo de PEEP está justo por encima del punto de inflexión inferior. Usando este enfoque, el nivel promedio de PEEP requerido es de 15 cm de agua.
Sin embargo, como se señaló anteriormente, un estudio de ARDS Network de niveles de PEEP más altos versus más bajos en pacientes con ARDS no encontró que los niveles más altos de PEEP fueran ventajosos. [ 47 ] En este estudio, el nivel de PEEP se determinó por la cantidad de oxígeno inspirado que se requería para lograr una saturación de oxígeno objetivo de 88-95% o una presión parcial de oxígeno (PO 2 ) objetivo de 55-80 mm Hg. El nivel de PEEP promedió 8 en el grupo de PEEP más bajo y 13 en el grupo de PEEP más alto. No se mostró ninguna diferencia en la duración de la ventilación mecánica o la supervivencia hasta el alta hospitalaria.
Una revisión de 2010 realizada por Briel et al. encontró que el tratamiento con niveles más altos de PEEP no demostró ninguna ventaja sobre el tratamiento con niveles más bajos en pacientes con ALI o SDRA; sin embargo, entre los pacientes con SDRA, los niveles más altos se asociaron con una mejor supervivencia. [ 54 ]
Un estudio de Bellani et al. encontró que en pacientes con ALI tratados con PEEP relativamente alta, la actividad metabólica de las regiones aireadas se asoció con la presión meseta y el volumen corriente regional que se normalizó por el volumen de gas pulmonar al final de la espiración; no se encontró asociación entre el reclutamiento/desreclutamiento cíclico y el aumento de la actividad metabólica. [ 55 ]
Ventilación controlada por presión y ventilación de alta frecuencia
Si se requieren presiones altas en las vías respiratorias inspiratorias para administrar incluso volúmenes corrientes bajos, se puede iniciar la ventilación controlada por presión (PCV). En este modo de ventilación mecánica, el médico establece el nivel de presión por encima de la CPAP (delta P) y el tiempo inspiratorio (tiempo I) o la relación inspiración/espiración (I:E). El volumen corriente resultante depende de la distensibilidad pulmonar y aumenta a medida que mejora el SDRA. La PCV también puede mejorar la oxigenación en algunos pacientes que no responden bien a la ventilación controlada por volumen (VCV).
Si la oxigenación es un problema, pueden resultar beneficiosos tiempos I más largos, de modo que la inspiración sea más larga que la espiración (ventilación con relación I:E inversa); se han utilizado relaciones de hasta 7:1. La ventilación con ventilación con presión máxima más baja también puede resultar beneficiosa en pacientes con fístulas broncopleurales, facilitando el cierre de la fístula.
La evidencia indica que la PCV puede ser beneficiosa en el SDRA, incluso sin las circunstancias especiales señaladas. En un ensayo controlado multicéntrico que comparaba la VCV con la PCV en pacientes con SDRA, Esteban descubrió que la PCV producía menos fallos en los sistemas orgánicos y tasas de mortalidad más bajas que la VCV, a pesar del uso de los mismos volúmenes corrientes y presiones inspiratorias máximas. [ 56 ] Se necesita un ensayo más amplio antes de hacer una recomendación definitiva.
La ventilación de alta frecuencia (jet u oscilatoria) es un modo de ventilación que utiliza volúmenes corrientes bajos (aproximadamente 1-2 ml/kg) y frecuencias respiratorias altas (3-15 respiraciones por segundo). Dado que se sabe que la distensión de los alvéolos es uno de los mecanismos que promueven la lesión pulmonar asociada a la ventilación, se esperaría que la ventilación de alta frecuencia fuera beneficiosa en el SDRA. Los resultados de los ensayos clínicos que comparan este enfoque con la ventilación convencional en adultos generalmente han demostrado una mejora temprana en la oxigenación, pero ninguna mejora en la supervivencia.
El ensayo controlado aleatorizado más grande incluyó a 548 adultos con SDRA de moderado a grave que fueron asignados aleatoriamente a ventilación convencional o ventilación oscilatoria de alta frecuencia (VOAF). Este estudio se interrumpió de manera temprana debido a un índice de mortalidad hospitalaria del 47 % en pacientes que recibieron VOAF y del 35 % en el grupo convencional. [ 57 ] Por lo tanto, no se recomienda la VOAF como estrategia de tratamiento para el SDRA.
También se ha probado la ventilación líquida parcial en el síndrome de dificultad respiratoria aguda. Un ensayo controlado aleatorio que la comparó con la ventilación mecánica convencional determinó que la ventilación líquida parcial resultó en un aumento de la morbilidad (neumotórax, hipotensión y episodios hipoxémicos) y una tendencia hacia una mayor mortalidad. [ 58 ]
Ventilación con liberación de presión de las vías respiratorias
La ventilación con liberación de presión de las vías respiratorias (APRV) es otro modo de ventilación que utiliza una duración prolongada (T alta) de una presión positiva alta en las vías respiratorias (P alta) seguida de una duración corta (T baja) a una presión baja (P baja). El tiempo transcurrido a una P alta en comparación con una P baja es una relación inversa a los patrones de respiración normales. Por ejemplo, un paciente puede pasar 5,2 segundos a una P alta y 0,8 segundos a una P baja. La teoría es que el tiempo transcurrido a una P alta aumenta y mantiene significativamente el reclutamiento alveolar, mejorando así la oxigenación. La APRV puede mejorar la oxigenación, pero no se han realizado ensayos controlados aleatorizados que demuestren una mejor supervivencia en el SDRA. Los médicos deben tener precaución con la APRV en pacientes con enfermedad pulmonar obstructiva, debido al tiempo de exhalación relativamente corto y la posible hiperinsuflación y barotrauma.
Posición boca abajo
Entre el 60 y el 75 % de los pacientes con SDRA mejoran significativamente su oxigenación cuando pasan de la posición supina a la prona. La mejora de la oxigenación es rápida y, a menudo, lo suficientemente sustancial como para permitir reducciones en la FiO2 o en el nivel de CPAP. La posición prona es segura, si se toman las precauciones adecuadas para asegurar todos los tubos y vías, y no requiere equipo especial. La mejora de la oxigenación puede persistir después de que el paciente vuelva a la posición supina y puede ocurrir en ensayos repetidos en pacientes que no respondieron inicialmente.
Los posibles mecanismos para la mejoría observada son el reclutamiento de zonas pulmonares dependientes, el aumento de la capacidad residual funcional (CRF), la mejora de la excursión diafragmática, el aumento del gasto cardíaco y la mejora de la correspondencia ventilación-perfusión.
A pesar de la mejora de la oxigenación con la posición prona, los primeros ensayos controlados aleatorizados de la posición prona en el SDRA no demostraron una mejor supervivencia. En un estudio italiano, la tasa de supervivencia al alta de la UCI y la tasa de supervivencia a los 6 meses no cambiaron en comparación con los pacientes que se sometieron a cuidados en posición supina, a pesar de una mejora significativa en la oxigenación. [ 59 ] Este estudio fue criticado porque los pacientes se mantuvieron en posición prona durante un promedio de solo 7 horas por día. Además, un estudio francés posterior, en el que los pacientes estuvieron en posición prona durante al menos 8 horas por día, no documentó un beneficio de la posición prona en términos de mortalidad a 28 o 90 días, duración de la ventilación mecánica o desarrollo de neumonía asociada al respirador (NAV). [ 60 ] Sin embargo, un ensayo controlado aleatorizado posterior en el que los pacientes con SDRA grave fueron colocados en posición prona de forma temprana y durante al menos 16 horas al día mostró un beneficio significativo en la mortalidad. [ 61 ] En este estudio, los pacientes con SDRA grave (PaO 2 /FiO 2 de < 150) fueron asignados aleatoriamente a posición prona después de 12-24 horas de estabilización. La tasa de mortalidad a los 28 días fue del 16% en el grupo prono y del 32,8% en el grupo supino. Los pacientes fueron girados manualmente. No se requirió una cama especializada.